2024 年 CNS(《Cell》《Nature》《Science》)期刊发表的新式卵白降解时期展现出了生物医学不绝范围的前沿进展,这些时期为深远泄露卵白质功能和疾病调整提供了强有劲的用具体育游戏app平台,底下让小编带群众回来下2024年发表在CNS上的新式卵白质降解时期。
01
转铁卵白受体靶向嵌合体(TransTACs)
细胞膜卵白的调控对细胞生理功能和疾病调整兴味紧要,但传统调控方法存在局限。2024年9月25日,Dana-Farber癌症不绝中心/哈佛大学医学院周昕团队在Nature期刊上发表了题为“Transferrinreceptor targeting chimeras for membrane protein degradation”的不绝论文(图1)。该不绝旨在确立一种新的膜卵白降解策略,以更灵验地调控膜卵白水温暖活性。
 图1.论文截图
图1.论文截图在该不绝中,不绝东谈主员发现转铁卵白受体1(TfR1)在癌细胞中过抒发且内吞作用马上,安妥用于靶向膜卵白降解。然后,不绝东谈主员打算了TF受体靶向嵌合体(TransTACs),其可运行靶卵白与TfR1共内化插足溶酶体降解阶梯(图2)。不绝标明,TransTACs能灵验降解多种膜卵白,如表皮滋长因子受体、活动性细胞圆寂1配体1等,降解后果在不同细胞系统中均开赴点80%。TransTACs还可用于胁制嵌合抗原受体(CAR)-T细胞活性,从而增强其抗肿瘤活性;能靶向肺癌中耐药的EGFR突变细胞,为癌症调整提供新策略。
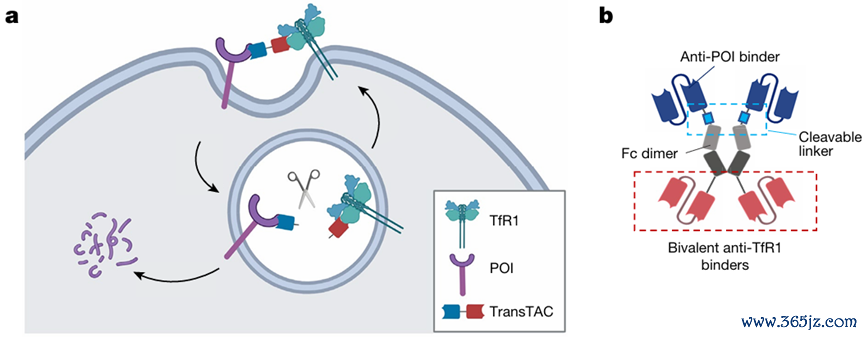 图2.TransTAC平台
图2.TransTAC平台TransTAC平台为膜卵白降解提供了新阶梯,有望在癌症调整等范围推崇紧要作用,为确立调整多种疾病的新方法提供了表面基础和本质依据。
02
基于trim21的分子胶和PROTAC降解剂(TrimTACs)
靶向卵白质降解是调整疾病的紧要策略,但现存方法依赖少数构成型活性的E3泛素相连酶,存在聘请性和药代能源学等问题。2024年11月1日,北京人命科学不绝所/清华大学生物医学交叉不绝院韩霆本质室与黄牛本质室配合在 Cell 期刊上发表了题为“Selective degradationof multimeric proteins by TRIM21-based molecular glue and PROTAC degraders ”的不绝论文(图3),该不绝通过寻找新的降解阶梯,以提升对多聚体卵白的降解聘请性和后果。
 图3.论文截图
图3.论文截图不绝东谈主员发现抗神经病药物阿立哌唑的代谢物(S)- ACE - OH可算作分子胶,指令E3泛素相连酶TRIM21与核孔卵白NUP98互相作用,导致核孔卵白降解和核质运输拦阻。基于此,不绝东谈主员打算了TRIM21 - basedPROTACs(TrimTACs),可聘请性降解生物分子凝华物中的多聚体卵白,而不影响单体卵白。不绝还通过晶体结构分析和生物物理测量,揭示了分子胶的作用机制和TRIM21与配体的诱骗形式。
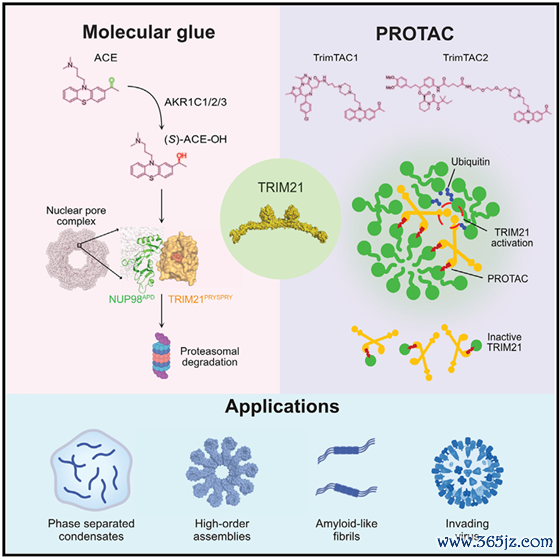 图4.TrimTAC平台
图4.TrimTAC平台TrimTACs平台为调整卵白质特地聚合关连疾病提供了新策略,有助于深远泄露卵白质降解机制,为确立针对多聚体卵白关连疾病的调整药物提供了新的想路和方法。
03
基于EndoTags的溶酶体靶向降解嵌合体(pLYTAC)
内吞作用和溶酶体运输是细胞名义受体调控的紧要机制,传统靶向降解方法存在局限性。2024年9月25日,卵白质打算前驱 David Baker教学团队与2022年诺贝尔化学奖得主CarolynBertozzi教学团队配合在 Nature期刊上发表了题为“Designedendocytosis-inducing proteins degrade targets and amplify signals”的不绝论文(图5),该不绝打算了新的内吞触发诱骗卵白(EndoTags),以克服传统方法的不及,从而结束更灵验的卵白质降解和信号调整。
 图5.论文截图
图5.论文截图在该不绝中,不绝东谈主员针对胰岛素样滋长因子2受体、去唾液酸糖卵白受体等受体打算了EndoTags,其与靶卵白诱骗剂交融后可指令受体构象变化或聚合,触发内吞作用,促进靶卵白的降解(图6)。同期,不绝东谈主员在此基础上构建了基于东谈主工打算卵白的溶酶体靶向降解嵌合体——pLYTAC,pLYTAC或者在活细胞中靶向降解无数疾病关连分子靶点,结束对靶卵白的溶酶体运输和靶向降解。由于这些受体卵白具有不同的组织漫步,因此,不同的EndoTag不错结束对不同组织的靶向降解。EndoTag的基因可编码性,使其可通过调整性mRNA或基因疗法寄递。在小鼠肿瘤模子中,EndoTag - 抗PD - L1交融卵白能权贵增强抗体的抗肿瘤活性。此外,EndoTags还可增强细胞内信号传导,如通过促进Notch - 养殖的合成信号系统的信号激活,结束信号的近100倍增强;之后,不绝东谈主员通过将多个EndoTag与卵白质开关LOCKR时期诱骗,创建了逻辑门控pLYTAC,结束更高特异性的卵白质靶向降解。
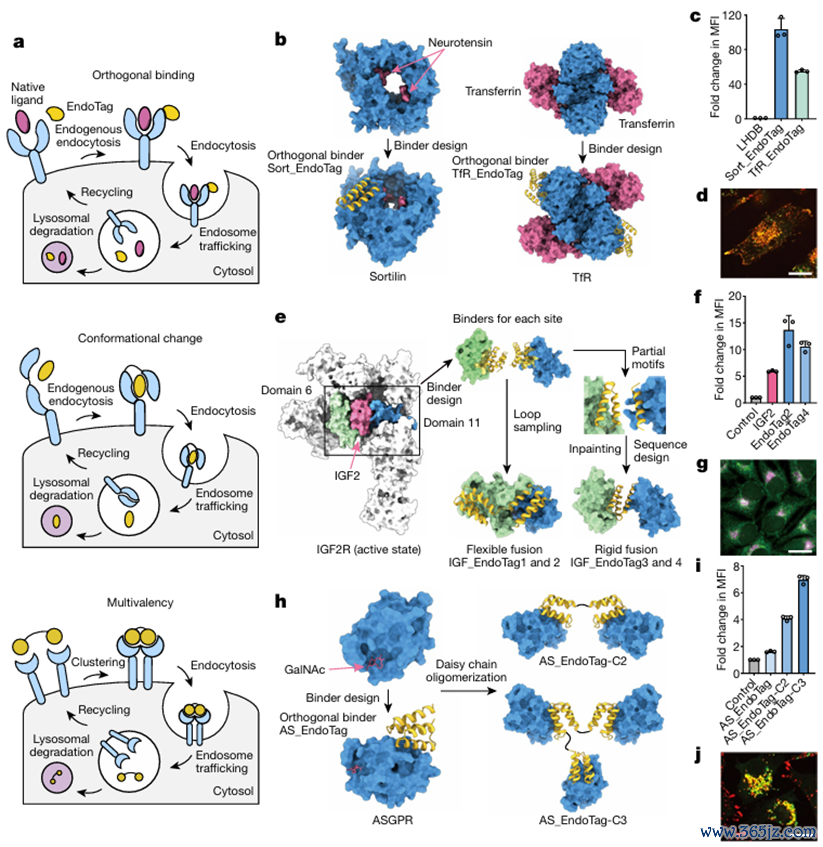 图6.内吞触发EndoTags的打算权术
图6.内吞触发EndoTags的打算权术EndoTags为卵白质降解和信号调整提供了转变的方法和策略,拓展了细胞内卵白质调控的技巧,为确立新式调整药物和调整多种疾病提供了新的阶梯和方法。
04
基于噬菌体接济的一语气进化(PACE)平台的锌指(ZF)降解子
小分子指令的降解子在基础不绝和临床应用中具有紧要兴味,但现存降解子存在一些问题,如大小不合适、对靶标卵白的特异性和亲和力不及等。2024年3月15日,麻省理工学院和哈佛大学Broad不绝所的刘如谦(David Liu)团队在 Science 期刊上发表了题为“Continuousevolution of compact protein degradation tags regulated by selective molecularglues”的不绝论文。该不绝基于噬菌体接济一语气进化(PACE)平台确立了一种新式靶向卵白质降解系统,以进化出更高效、特异性更强的降解子。
 图7.论文截图
图7.论文截图在该不绝中,不绝东谈主员开赴点构建了噬菌体接济的一语气进化(PACE)平台,用于筛选和进化与分子胶复合物互相作用的卵白质。行使该系统,从锌指(ZF)卵白和分子胶构成的复合物中筛选出了或者与CRBN诱骗的ZF降解子,并对其进行了优化,取得了SD40等高效降解子(图8)。SD40仅36个氨基酸,可通过prime editing高效插入基因组位点,对其靶卵白具有高效、快速和聘请性的降解才气。不绝还理会了SD40与CRBN诱骗的复合物结构,揭示了其作用机制和特异性。此外,针对小鼠CRBN中存在的突变,进化出了SD56等能在小鼠细胞中推崇作用的降解子。
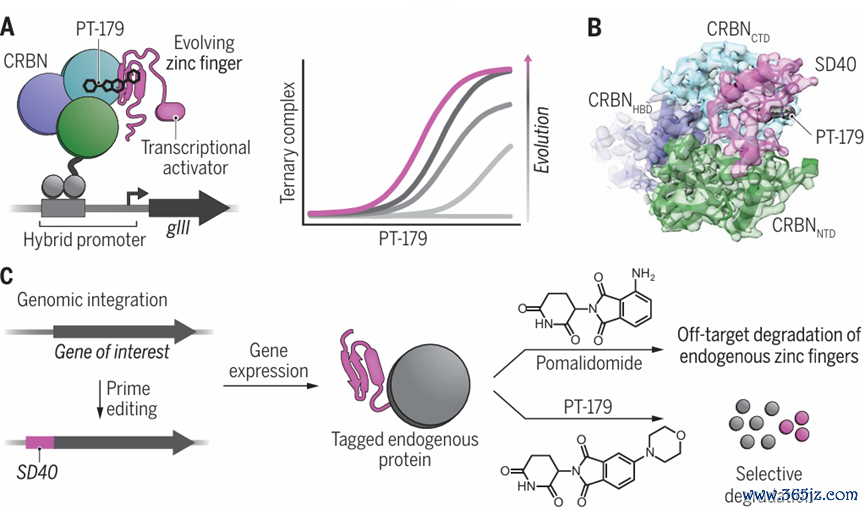 图8.新式锌指结构域提醒其秀雅的内源性卵白的特异性降解
图8.新式锌指结构域提醒其秀雅的内源性卵白的特异性降解总之,该不绝确立的PACE系统为快速进化分子胶复合物提供了有劲用具,进化取得的ZF降解子为卵白质降解和靶向调整范围提供了新的想路和方法,有助于鼓舞关连范围的不绝和应用。
05
分子内二价胶水(IBGs)
靶向卵白质降解是一种紧要的调整策略,但现在的方法如PROTACs和分子胶等存在一些局限性,如需要与靶标卵白和E3泛素相连酶诀别诱骗、对靶标卵白的聘请性和降解后果有待提升档。2024年2月21日,英国邓迪大学人命科学学院靶向卵白降解不绝中心与奥地利科学院CeMM分子医学不绝中心配合在Nature期刊上发表了题为“Targetedprotein degradation via intramolecular bivalent glues”的不绝论文,该不绝揭示了一类全新的靶向卵白降解分子—分子内二价胶(intramolecularbivalent glues,IBG),这类分子的降解形式诱骗了PROTAC和分子胶的特质,或者结束低皮摩尔着力的降解,有望开启新一代的TPD调整形式。
 图9.论文截图
图9.论文截图在该不绝中,不绝东谈主员发现了一种新式的双功能降解剂—分子内二价胶(IBGs),它或者同期与靶标卵白的两个相邻结构域诱骗,指令靶标卵白的降解。以IBG1为例,它能灵验降解BRD2和BRD4,但不降解BRD3,其作用依赖于CRL4 - DCAF16复合物。不绝东谈主员通过多种本质时期不绝了IBG1的作用机制,发现IBG1能增强DCAF16与BRD4的亲和力,使两者酿成泄露的三元复合物,促进BRD4的泛素化和降解。基于机制和结构的泄露,不绝东谈主员对IBG1进行优化,取得了IBG3等更高效的降解剂,其降解后果可达皮摩尔浓度。
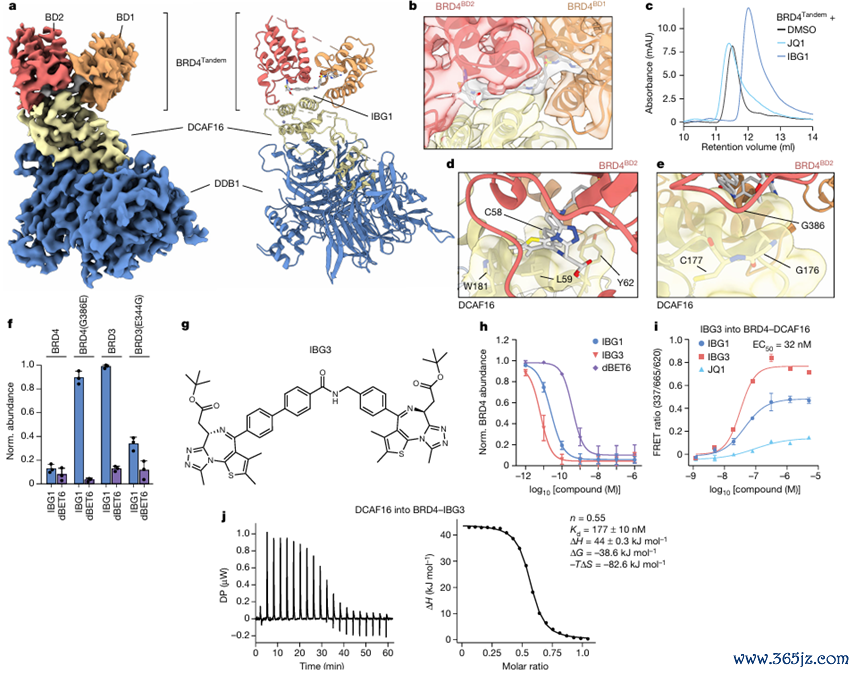 图10.IBG1同期参与BRD4的两个溴结构域,并将BRD4粘合到DCAF16上
图10.IBG1同期参与BRD4的两个溴结构域,并将BRD4粘合到DCAF16上不绝发现的IBGs为靶向卵白质降解提供了一种新的策略,具有高效、聘请性强等优点,为调整癌症等疾病提供了新的调整技巧,也为进一步泄露卵白质-卵白质互相作用和靶向卵白质降解机制提供了紧要的表面依据。
06
结语
这些新式卵白降解时期为疾病调整提供了新的想路和方法。举例,IBGs 和 TransTACs 等时期可用于靶向降解与疾病关连的卵白质,如癌症细胞中的特定卵白靶点,为癌症调整提供了更灵验的调整技巧。同期,新式卵白降解时期的发展也为药物研发带来了启示。通过打算和优化降解子,不错提升药物的特异性和疗效,减少药物的反作用。此外,这些时期还不错用于发现新的药物靶点和调整药物,为药物研发范围的转变发展提供了紧要的相沿。
Ref.
[1]Zhang,Dingpeng et al. “Transferrin receptor targeting chimeras for membrane proteindegradation.” Nature,10.1038/s41586-024-07947-3.
[2]Lu, Panrui etal. “Selectivedegradation of multimeric proteins by TRIM21-based molecular glue and PROTACdegraders.” Cell vol.187,25 (2024): 7126-7142.e20.
[3]Huang, Buweiet al. “Designedendocytosis-inducing proteins degrade targets and amplify signals.” Nature,10.1038/s41586-024-07948-2.
[4]Mercer, JaronA M et al. “Continuousevolution of compact protein degradation tags regulated by selective molecularglues.” Science (NewYork, N.Y.) vol. 383,6688 (2024): eadk4422.
[5] Hsia, Oliver et al. “Targeted protein degradation via intramolecularbivalent glues.” Nature vol. 627,8002 (2024): 204-211.
 ]article_adlist-->
]article_adlist-->(转自:抗体圈)体育游戏app平台
 海量资讯、精确解读,尽在新浪财经APP
海量资讯、精确解读,尽在新浪财经APP



